- Deshidratación de alcoholes
Los éteres alifáticos simétricos pueden obtenerse por deshidratación de alcoholes , mediante la acción del ácido sulfúrico. Este es uno de los métodos comerciales de preparación del éter ordinario, dietiléter, por lo que se llama frecuentemente éter sulfúrico.Se lleva a cabo tratando el alcohol con ácido sulfúrico a 140°. La deshidratación es intermolecular:
|
|
H2SO4
140º |
H2O + CH3—CH2—O—CH2CH3 |
| etanol |
|
dietiléter |
Este proceso se ve fácilmente afectado por reacciones secundarias, como la formación de sulfatos de alquilo (especialmente si baja la temperatura), y la formación de olefinas (especialmente si sube la temperatura).
La deshidratación de alcoholes puede también realizarse en fase vapor, sobre alúmina a 300°, aunque este procedimiento sólo es satisfactorio con alcoholes primarios, ya que los secundarios y los terciarios dan lugar a la formación de olefinas.
- A partir de alcoholatos (Síntesis de Williamson)
Los alcoholatos dan lugar a la formación de éteres al ser tratados con halogenuros de alquilo según:
|
|
IR’ |
|
R—O—R’ + NaI |
| alcoholato |
halogenuro
de alquilo |
éter |
![[small][AnimePaper]wallpapers_Ergo-Proxy_Tenken-the-2nd(1_33)__THISRES__73653 [small][AnimePaper]wallpapers_Ergo-Proxy_Tenken-the-2nd(1_33)__THISRES__73653](https://kira2629.files.wordpress.com/2009/06/smallanimepaperwallpapers_ergo-proxy_tenken-the-2nd1_33__thisres__73653.jpg?w=477&h=86)
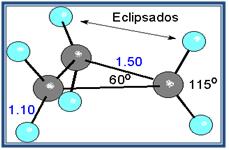
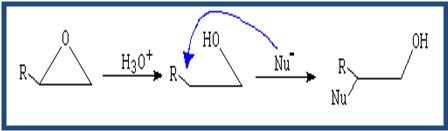
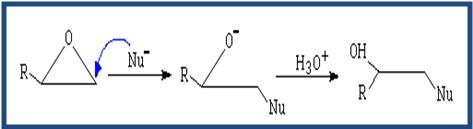 ( Apertura por neoclófilo) El neoclófilo ataca al carbono menos sustituido.
( Apertura por neoclófilo) El neoclófilo ataca al carbono menos sustituido.